 복지부 제공
복지부 제공혁신적 의료기기가 신의료기술평가를 거치지 않고 최단 80일 만에 의료현장에 진입할 수 있는 제도가 시행된다.
26일 보건복지부와 식품의약품안전처에 따르면 두 부처는 '시장 즉시진입 의료기술' 제도를 이날부터 시행한다.
이 제도는 식약처의 의료기기 허가 단계에서 국제적 수준의 강화된 임상평가를 거친 의료기기를 활용한 의료기술에 대해 별도의 신의료기술평가 없이 의료현장에서 사용할 수 있도록 한 것이 핵심이다. 관련 내용을 담은 '신의료기술평가에 관한 규칙'과 '의료기기 허가·신고·심사 등에 관한 규정' 개정 절차도 마무리됐다.
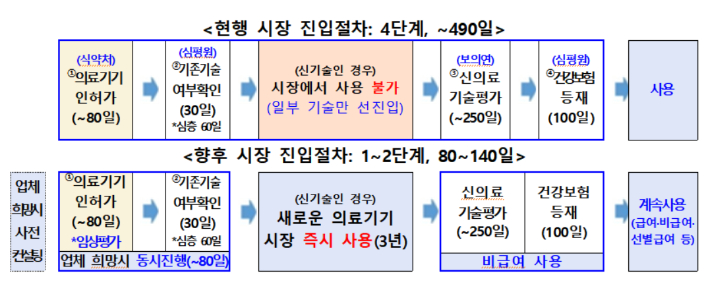
그동안 새로운 의료기술은 △의료기기 인허가 △기존기술 여부 확인 △신의료기술평가 △건강보험 등재 등 4단계를 거쳐야 해 최대 490일이 소요됐다. 이번 제도 시행으로 해당 절차는 1~2단계로 축소돼 시장 진입 기간이 최단 80일까지 단축된다.
시장 즉시진입 의료기술로 지정되면 의료현장에서 최대 3년간 사용할 수 있으며, 이후 신의료기술평가와 건강보험 급여 여부 결정 절차를 거치게 된다. 즉시진입 사용 기간 중에도 필요할 경우 보건복지부 장관이 직권으로 신의료기술평가를 실시해 비급여 관리와 환자 안전을 점검할 수 있도록 했다.
식약처는 복지부와 협의해 시장 즉시진입 대상 의료기기 품목도 공고했다. 대상에는 디지털의료기기 113개 품목, 체외진단시약 83개 품목, 의료용 로봇 등 기타 품목을 포함해 총 199개 품목이 포함됐다.
복지부와 식약처는 제도 시행과 함께 비급여 사용 현황을 관리하고, 안전성과 유효성이 확인되지 않은 의료기술은 시장에서 배제하는 등 관리 체계를 병행해 운영할 계획이다.
복지부 곽순헌 보건의료정책관은 "안전하지 않은 의료기술은 시장에서 퇴출하고, 환자부담 완화를 위해 비급여 사용현황을 모니터링해 새로운 제도가 의료현장에 정착될 수 있도록 관계기관과 지속 협력하겠다"고 밝혔다.